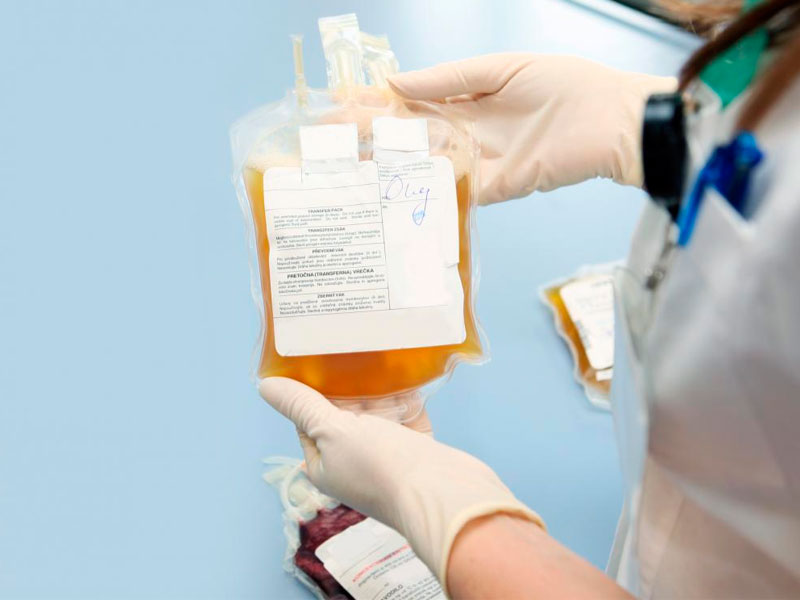
Dos resoluciones del Ministerio de Salud que regulan en qué momento de la enfermedad por coronavirus es recomendable aplicar plasma de convaleciente y suero equino -elaboradas en consenso junto a especialistas de diferentes sociedades científicas e investigadores de ensayos clínicos que se realizaron en el país con ambos tratamientos- fueron publicadas hoy en el Boletín Oficial.
La resolución firmada por la Secretaria de Calidad de Salud que regula la recomendación de plasma de pacientes recuperados, lleva el número 9/2021 e indica que debe administrarse como tratamiento en pacientes con menos de tres días de iniciados los síntomas, que no presenten criterios de gravedad y con diagnóstico confirmado de Covid-19.
En ese contexto, se establecieron además cinco condiciones: la primera que el tratamiento «debe realizarse de acuerdo al criterio de los médicos tratantes en interconsulta con el Servicio de Medicina Transfusional en el marco de Protocolos médicos aprobados por la Autoridad Jurisdiccional correspondiente».
También se indicó que «se debe indicar la transfusión de Plasma de convaleciente de Covid-19 en pacientes mayores de 75 años con menos de 72 horas de iniciados los síntomas».
Como tercera observación se fijó el mínimo y el tipo de anticuerpos que tiene que tener el plasma que se utilizará como tratamiento y los métodos validados para confirmar estas condiciones del plasma: «Deben contar con títulos de IgG anti-SARSCoV-2 superiores a 1:1000, obtenidos por el método CoviDAR o un s/CO ≥ 5.0 si se utilizan métodos de ELISA/CMIA de sensibilidad equivalente y autorizados por la autoridad competente».
Además, se señaló que «las unidades de plasma a transfundir deben poseer en la etiqueta el valor de la concentración de anticuerpo».
Por último, se fijó como referencia que se debe transfundir una unidad de plasma de convaleciente de volumen entre 200 y 300 mililitros, con las características mencionadas anteriormente.
La resolución también indicó que no se debe administrar plasma de convaleciente a pacientes con más de tres días de iniciados los síntomas o con alguna de las siguientes características: frecuencia respiratoria mayor a 30/min, saturación de oxígeno menor de 93% respirando aire ambiente, pacientes con enfermedad grave, gestantes o menores de 18 años.
Participaron en la elaboración de estas recomendaciones especialistas de la Asociación Argentina de Hemoterapia, Inmunohematología y Terapia Celular (AAHITC), del Grupo Cooperativo Iberoamericano de Medicina Transfusional. (GCIAMT), de la Sociedad Argentina de Infectología (SADI), del Consorcio de Instituciones coordinada por el Hospital Italiano de Bs As, Fundación Infant y Dirección de Medicina Transfusional del Ministerio de Salud.
En referencia a las inmunoglobulinas equinas, conocidas como suero equino, la resolución lleva el número 8/2021 y se advirtió que estas indicaciones «se encuentran en revisión permanente y están sujetas a actualizaciones según la evidencia científica disponible».
La resolución recomendó considerar la «administración de inmunoglobulinas equinas fragmentos F (ab)2 anti SARS-CoV-2 en pacientes con enfermedad severa hasta 10 días desde el inicio de síntomas, con diagnóstico confirmado de Covid-19».
En relación a las condiciones, se estableció que el tratamiento debe realizarse en pacientes con enfermedad severa según los criterios del Instituto Nacional de Salud de los Estados Unidos: «Pacientes con SaO2 (saturación de oxígeno) <94% con aire ambiental o PaFIO2 (relación entre la presión arterial de oxígeno y la fracción inspirada de oxígeno) <300, frecuencia respiratoria >30 por minuto, o infiltrados pulmonares > 50%».
También se estableció que debe ser administrada en ámbito hospitalario con monitoreo médico y se deben indicar dos dosis a razón de 4 mg/Kg de peso con un intervalo de 48 horas por vía intravenosa.
Además, la resolución estableció que no se debe indicar suero equino como tratamiento en pacientes internados internados en la Unidad de Terapia Intensiva, es decir de curso crítico de acuerdo a la definición de los Institutos Nacionales de Salud (NIH) ni en pacientes con requerimiento de Asistencia Respiratoria Mecánica (ARM).
Tampoco se debe indicar en personas con antecedentes de anafIlaxia, administración previa de suero equino (por ejemplo que hayan recibido suero antitetánico, antiofídico o antitoxina arácnida) o una reacción alérgica por contacto o exposición a los caballos».
Por otra parte, tampoco está recomendado indicar en pacientes que causan enfermedad leve o moderada, ni que hayan recibido plasma de convalecientes.
En tanto que para personas que estén gestando, en etapa de lactancia o en menores de 18 años tampoco está recomendado.
Estas recomendaciones fueron el resultado de un consenso al que llegaron especialistas de diferentes sociedades científicas como la Sociedad Argentina de Infectología (SADI), la Sociedad Argentina de Terapia Intensiva (SATI), la Sociedad Argentina de Medicina (SAM) e investigadores que participaron de ensayo clínico. investigadores independientes y especialistas del Ministerio de Salud.
El suero equino contra el coronavirus son anticuerpos policlonales desarrollado por científicos argentinos producto de una articulación público-privada encabezado por el laboratorio Inmunova y el Instituto Biológico Argentino (BIOL), la Administración Nacional de Laboratorios e Institutos de Salud Carlos G. Malbrán (ANLIS), con la colaboración de la Fundación Instituto Leloir (FIL), Mabxience, CONICET y la Universidad Nacional de San Martín (UNSAM).
En diciembre, ANMAT lo aprobó como tratamiento a partir de los resultados positivos del estudio clínico de Fase 2/3, los cuales mostraron que la aplicación de esta terapia, además de ser segura, redujo la mortalidad casi a la mitad (45%) en los pacientes con COVID-19 severa.
Además, los pacientes tratados demostraron una reducción de la internación en terapia intensiva de 24% y del requerimiento de asistencia respiratoria mecánica de 36%, frente al placebo.
En relación al plasma de convalecientes, que se ha utilizado ya en la historia por ejemplo contra la fiebre amarilla, varios estudios indicaron beneficios si se administra en etapas tempranas de la enfermedad.
En Argentina, se realizaron al menos cuatro estudios con plasma: el liderado por el CEMIC, el del Hospital Italiano, el de la Fundación Infant y el que estuvo encabezado por el Ministerio de Salud de la Provincia de Buenos Aires.
A excepción del ensayo clínico del Italiano, que trabajó con pacientes hospitalizados con neumonía por Covid-19 con criterios de gravedad y no encontró diferencias significativas entre los que recibieron plasma y los que recibieron placebo, el resto de los estudios arrojaron resultados buenos para el plasma en cuanto a la reducción de la mortalidad y la progresión a cuadros más severos de la enfermedad.